PENGENDALIAN MIKROBA
7.1. Definisi dari
istilah yang sering digunakan.
Terminologi
sangat penting dalam pengendalian mikroorganisme dimana penggunakan kata
disinfectant dan antiseptic sering digunakan. Keadaan dapat lebih membingungkan
Karena penangan secara khusus dapat menumbuhkan ataupun membunuhnya tergantung
pada kondisi tertentu.
Kemampuan untuk mengendalikan populasi mikroba pada
benda mati, seperti alat makan dan alat operasi sangatlah penting. Terkadang
sangat penting untuk melenyapkan seluruh mikroorganisme pada objek tersebut. Sterilisasi (Bahasa latin “sterilis”, tidak dapat berkembang atau
mandul adalah
suatu proses dimana seluruh sel yang hidup, baik itu spora, virus dan viroid dilenyapkan dari suatu objek atau
habitat. Objek yang steril tidak memiliki mikroorganisme, spora dan senyawa
penginfeksi lain didalamnya. Ketika keadaan steril dicapai menggunakan
perantara kimia, maka senyawa kimia disebut sterilant.
Berlainan dengan ini, Desinfeksi adalah membunuh,
menghancurkan atau melenyapkan mikroorganisme yang dapat menyebabkan penyakit.
Tujuan utamanya dalah untuk menghancukrkan pathogen, damun desinfeksi juga
mengurangi jumlah mikroba. Desinfectant adalah
agen/perantara, umumnya berupa senyawa, yang digunakan untuk mengangkut spora
dan beberapa mikroorganisme yang masih tersisa. Sanitization berkaitan dengan desinfeksi. Dalam sanitasi, populasi
mikroba dikurangi sehingga
mencapai level dimana mikroba dianggap tidak berbahaya bagi kesahatan. Benda
mati umumnya dibersihkan dan di desinfeksi secara sebagian. Misalnya, Sanitizer yang digunakan untuk alat
makan pada restoran.
Sangatlah penting bagi kita secara sering mengontrol
mikororganisme pada kulit/jaringan tubuh dengan perantara kimia. Antisepsis (Yunani: anti, melawan, sepsis, pembusukan) adalah mencegah infeksi atau kebusukan dan
dapat dicapai menggunakan antiseptik.
Antiseptik
merupakan perantara kimia yang dioleskan pada kulit/jaringan guna mencegah
infeksi dengan cara memangkas pertumbuhan pathofen; antiseptic juga mengurangi
jumlah mikroba. Karena antiseptic tidak menghancurkan inang dari kulit,
antiseptic tidak beracun seperti disinfectant.
Sebuah akhiran dapat dipakai untuk menandai tipe-tipe
perantara antimikroba. Zat yang dapat membunuh organisme sering diberik akhiran
-cide (latin: Cida, membunuh). Germicide membunuh pathogen tetepi tidak endospores. Disinfectant atau antiseptic
daapt bekerja secara efektif pada suatu kelompok, yaitu bactericide, fungicide,
algicide, atau viricide. Senyawa kimia lain yang tidak membunuh, tetapi memperlambat
pertumbuhan. Apabila senyawa perantara ini dihilangkan, maka pertumbuhan akan
berlanjut. Senyawa/zat ini ditambahi akhiran -static (Yunani: statikos,
menyebabkan sesuatu berhenti) misalnya bacteriostatic
dan fungistatic.
Meski perantara ini dijelaskan berdasar efeknya
terhadap pathogen, harus tetap dicatat bahwa merea juga membunuh atau
memperlambat zat nonpathogen juga. Kemampuan mereka dalam mengurangi populasi
mikroba, tidak hanya berpengaruh di tingkat pathogen, namun juga sangat penting
dalam situasi tertentu.
7.2 Pola Kematian Mikroba
Populasi mikroba tidak terbunuh secara instan ketika
terkena senyawa yang letal/mematikan. Matinya populasi, seperti halnya
pertumbuhan popuasi seringnya terjadi secara bertingkat/algoritme, karenanya
populasi akan terus berkurang
dengan interval yang konstan (Tabel 7.1). apabila algoritme dari total populasi
dibandingkan dengan lamanya waktu terkena agen perantara kimia tersebut, maka
dapat ditarik garis lurus. (bandingkan gambar 7.1 dengan gambar 6.2). ketika
populasi berkurang secara drastis, jumlah yang terbunuh akan berkurang dikarenakan
mikroorganisme yang tersisa memiliki daya tahan yang lebih kuat.
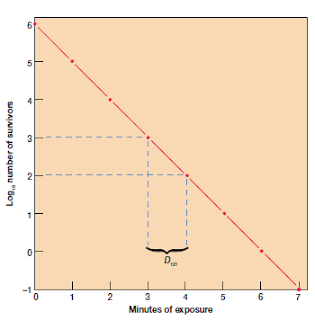
Gambar 7.1
Pola Kematian mikroba. Garis exponential dari mikroorganisme tersisa berbanding
dengan lamanya waktu terkena panas pada 121 C. pda contoh D121
valuenya adalah 1 menit. Data diambil dari table 7.1.
Tabel
7.1 Teori dalam membunuh mikroba menggunakan
panas.
Guna mempelajari efektifitas dari senywa mematikan,
kita harus menentukan kapan mikroorganisme akan mati, tugas ini tentunya tidak
mudah. Sangat sulit bahkan tidak mungkin kita mengecek denyut nadi bakteri.
Bakteri dianggap mati apabila ia tidak bertumbuh atau berproduksi ketika
diletakkan pada wadah yang dapat meningkatkan pertumbuhannya.
7.3
Pengaruh kondisi dan Efektifitas dari aktifitas agen antimikroba
Penghancuran mikroorganisme dan pengekangan
pertumbuhannya bukan masalah sepele, Karena efesiensi dari antimicrobial agent (perantara yang dapat membunuh atau mengekang
pertumbuhannya) dipengaruhi oleh 6 faktor :
1. Ukuran populasi. Karena sejumlah
fraksi populasi mikroba terbunuh setiap intervalnya, maka populasi yang lebih
besar cenderung memakan waktu lebih lama. Seperti pada tabel dan gambar 7.1.
2.
Komposisi dari populasi.
Efektifitas suatu agent bervariasi tergantung dari bagaimana organisme
diperlakukan, Karena mikroorganisme dibedakan dengan kerentanannya. Bakter
endospore lebih resistan, sel yang muda umumnya lebih mudah dihancurkan. Bahkan
ada beberapa spesies yan sangat sulit dihancurkan. Mycrobactium tuberculosis, yang menyebabkan tuberkolosis, lebih
resistan terhadap senyawa pembunuhnya dibanding dengan bakteri lain.
3. Konsentrasi dan
intensitas dari agent antimikroba. Sering, namun tidak selalu, senyawa dengan
konsentrasi tinggi lebih cepat menghancurkan mikroorganisme. Namun, keefektifannya
biasa tidak secara langsung berhubungan dengan konsentrasi atau intensitas.
Misalnya. 70% etanol lebih efektif dibanding 95% etanol dikarenakan adanya
kehadiran dari air.
4. Lamanya terjangkit.
Semakin lama populasi terkena agen antimicrobe, lebih banyak pula organisme
yang dibunuh (gambar 7.1). untuk mencapai keadaan steril, durasi pemaparan harus dikurangi dengan probabilitas dari
survival yaitu 10-6 atau lebih kecil.
5. Temperatur. Peningkatan
temperature pada suatu senyawa sering meningkatkan aktifitasnya. Umumnya
kosentarsi rendah dari disinfectant atau agen sterilisasi dapat dipakai pada
suhu lebih tinggi.
6. Lingkungan sekitar.
Populasi yang akan dikontrol tidak pada keadaan isolasi namun dikelilingi oleh
faktpr lingkungan yang mungkin dapat melindungi dari kehancuran. Misalnya,
Karena panas dapat membunuh lebih cepat pada pH asam, makanan asam dan minuman
seperti buah dan tomat lebih mudah di pasterisasi dibanding makanan dengan pH
tinggi seperti susu.
7.4 Penggunaan Metode Kontrol
Secara Fisik
Panas dan agent fisikal lainnya sering
digunakan untuk mengontrik pertumbuhan mikroba dan mensterilisasi suatu objek,
seperti terlihat pada operasi secara berlanjut dari autoclave di lab
mikrobiologi. Agent fisikal yang paling sering digunakan adalah, panas, temperature
rendah, filtrasi dan radiasi.
Heat (Panas)
Api dan memanaskan air dapat dipakai untuk sterilisasi
dan disinfeksi sejak jaman Yunani, pemanasan adalah cara paling popular dalam
menghancurkan mikroorganisme. Baik moist
heat maupun dry heat.
Moist heat
secara cepat membunuh virus, bakteri dan jamur (tabel 7.2). pemaparan pada air
mendidih selama 10 menit sudah cukup untuk menghacurkan sel vegetative dan
spora eukaryotic. Sayangnya temperature dari air mendidih (100oC)
tidak cukup tinggi untuk membunuh bakter endospore yang dapat bertahan setelah
berjam-jam direbus. Oleh Karena itu perebusan dapat dipakai dalam disfensi
minuman dan objek yang tidak berbahaya bagi air, namun perebusan tidak
mensterilisasi.
Karena pemaparan pada air mendidih selama 10 menit
sudah cukup untuk menghacurkan sel vegetative dan spora eukaryotic
Tabel 7.2
Perkiraan kondisi pada pembunuhan dengan Moist
Heat
Gambar 7.2 Perhitungan
nilai. z value digunakan dalam perhitungan
hubungan suhu dengan temperature terhadap ketahanan mikroorganisme, berdasarkan
dari respon D value pada berbagai suhu. z value adalah peningkatan suhu yang
dibutuhkan untuk mengurangi waktu pengurangan decimal (D) menjadi 10% dari nilai awalnya. Untuk sampel homogenous dari uji
mikroorganisme ini didapat z value sebesar 10.5o. D value digambarkan dalam skala
algoritme.
Awalnya keefektifan sering digambarkan dengan Thermal Death Point (TDH) atau titik
panas kematian, pada suhu terendah, mikroba dapat dibunuh dalam 10 menit.
Karena TDP mengesankan kita bahwa pada suatu titik temperature dianggap
mematikan dalam kondisi apapun. Thermal
Death Time (TDT) waktu keamatian terhadap panas, lebih sering digunakan
sekarang ini. Karena waktu tersingkat yang dibutuhkan untuk membunuh semua
organisme mikroba adalah pada temperature tertentu dan pada kondisi yang telah
ditentukan. Namun, penghancuran tersebut tidak algoritme, dan secara teori
tidak mungkin untuk menghancurkan secara total mikroorganisme pada sampel.
Meski dengan pemanasan yang ditambah. Oleh Karena itu gambaran yang lebih rinci
atau tepat, decimal reduction time (D) atau Value D telah diterima
secara umum. D adalah waktu yang
dibuthkan untuk membunuh 90% mikroorganisme atau spora pada sampel dalam suhu
tertentu. Value D adalah waktu yang
dibutuhkan untuk garis agar turun 1 log putaran. Value D biasanya ditulis dengan subscript, mengindikasikan suhu yang
dipakai. Value D digunakan untuk
mengestimasi resistan secara relative dari suatu mikroorganisme pada suhu
berbeda melalui perhitungan z value. z
value adalah meningkatnya suhu yang dibutuhkan untuk mengurangi D dari 1/10
jumlah awalnya atau mengurangi 1 log atau 1/10 nya. (gambar 7.2). cara lain
untuk menggambarkan efektifitas pemanasan adalah menggunakan F value yaitu waktu
dalam satuan menit pada suhu tertentu (biasanya 121,1oC atau 250oF)
yang dibutuhkan untuk membunuh populasi sel atau spora.
Pemrosesan makan pada pabrik menggunakan D dan z value. Setelah makanan
dikalengkan, maka harus dipanaskan guna mengeliminasi resiko peningkatan botulism dari spora Clostridium botulinum. Pemanasan dilakukan selama mungkin guna
mengurangi populasi sebanyak 1012 spora C. botulinum menjadi 100 (1 spora), karenanya ada
kemungkinan kecil terdapat spora yang masih berbahaya. Value D untuk spora ini pada suhu 121oC
adalah 0,204 menit. Oleh Karena itu akan memakan 12 D
atau 2.5 menit untuk mengurangi 1012 spora menjadi 1 spora dengan
pemanasan pada suhu 121oC. value z dari spora C. botulinum adalah 10oC, karenanya akan 10oC
suhu harus diubah untuk mengubah nilai D
value 10x lipat. Apabila kaleng diprses pada 111oC dibanding dengan
121oC, maka value D akan
meningkat 10 x
dari 2.04 menit dan 12 value menjadi 24.5 menit. Value D dan value z untuk jenis pathogen pada makanan umum terdapat pada
tabel 7.3. tiga value D dimasukkan
untuk Staphylococcus aureus untuk
mengilustrasikan variasi tingkat pembunuhan dan lingkungan dengan efek
melindungi bagi material organic.
Moist heat sterelisasi
harus dilakukan pada suhu diatas 1000C guna menghancurkan bakteri
endospore, dan ini dapat dicapai menggunakan uap pada tekanan. Sterilisasi
menggunakan uap dapat dilakukan dengan Autoclave
(gambar 7.3), sebuah alat semacam penanak nasi. Pengembangan autoclave yang
dimulai pada 1884 dapat menstimulasi pertumbuhan mikrobiologi. Air dipanaskan
menghasilkan uap, yang kemudian dilepaskan menuju kamar autoclave. Udara yang
awalnya ada pada kamar tersebut dipaksa keluar hingga kamar berisi dengan uap
kemudian outlet ditutup. Panas. Uap panas kemudian masuk hingga uap mencapai
suhu tertentu dan tekanan tertentu, biasanya 121oC dan 15 pound
tekanan. Pada suhu ini, uap jenuh menghancurkan semua cel vegetative dan
endospore pada volume cairan yang rendah sekitar 10 – 12 menit. Proses akan
berlangsung hingga 15 menit dan menghasilkan titik aman. Tentunya wadah yang
lebih besar dari cairan sperti wadah labu botol akan memakan waktu lebih lama.
Moist heat
dapat membunuh secara efektif dan menurunkan asam cleic dan mengubah sifat
enzim dan protein lainnya. Ia juga dapat merusak sel membrane.
Autoclaving harus dilakukan secara benar atau material
yang diproses tidak akan steril. Apabila seluruh udara tidak dikeluarkan dari
kamar, suhu tidak akan mencapai 121oC meski tekanan mencapai 15
pounds. Kamar/ruang tidak harus terlalu padat Karena uap butuh bersirkulasi
secara bebas agar berkontak dengan
seluruh bagian autoclave. Bakteri endospore akan terbunuh apabila suhu tetap
121oC selama 10 – 12 menit. Ketika volume cairan yang besar harus
disterilkan, dibutuhkan waktu tambahan untuk mencapai suhu 121oC; 5
liter cairan membutuhkan waktu 70 menit. Dalam mengatasi masalah ini, indicator
biologis sering di autoclave bersamaan dengan material lain. Indicator ini
umumnya terdiri dari tabung sampel yang megandung waduh ampul yang steril yaitu
kertas yang terdapat spora dari Bacillus
stearithermophilus atau Clostridium PA3679
setelah autoclaving, ampul akan patah secara aseptic dan tabung akan diinkubasi
selama beberapa hari. Apabila bacteri yang di uji tidak tumbuh dalam medium,
maka sterilisasi dianggap sukses. Terkadang digunakan kertas special yang
bertuliskan steril atau kertas indicator yang berubah warna apabila suhu
autoclave mencapai titik tertentu. Apabila kata tersebut muncul atau warna
berubah setelah proses autoclave, maka material harusnya steril. Pendekaatan
ini dianggap mudah dan menghemat waktu namun tidak ampuh digunakan untuk
bakteri endospore.
Tabel 7.3
D value dan z value dari beberapa
makanan mengandung Pathogen
Gambar 7.3 Autoclave dan
Steam Sterilizer. (a) autoclave atau sterilizer
dengan control otomatis yang modern. (b) Longitidal cross section dari
autoclave pada umumnya, menunjukkan beberapa bagian dari jalur masuk uap. (b)
dari John J. Perkins, metode dan prinsip dari sterilisasi pada sains kesehatan,
edisi 2, 1969.
Banyak zat, seperti susu diproses dengan mengontrol
panas pada suhu sedikit dibawah titik didih, proses ini disebut pasteurization dinamai atas
pengembangnya Lousi Pasteur. Pada 1860 di industry wine prancis menghadapi
masalah terbuang/basinya wine yang menyebabkan penyimpanan wine dan
pengirimannya menjadi sulit. Pasteur kemudian meneliti wide tersebut dengan
mikroskop dan mendeteksi adanya mikroorganisme yang sepert bakteri yang
menyebabkan asam lactic dan asam acetic terfermentasi. Ia kemudian menemukan
bahwa pemanasan pada suhu 55-60oC akan membunuh mikroorganisme ini
dan dapat mengawetkan wine dalam priode waktu lama. Pada 1886 ahli kimia jerman
V.H. dan F. Soxhlet menggunakan teknik ini untuk mengawetkan susu dan
mengurangi penyakit Karena susu yang basi. Pasteurisasi susu dikenalkan di U.S
pada 1889. Susu, bir dan berbagai minuman lain sekarang dipasteuraisasi. Pasteurisasi
tidak mensterilkan minuman, namun ia membunuh pathogen yang terdapat didalamnya
dan melambatkan basinya produk dengan cara mengurangi tingkat terbuangnya
mikroorganisme nonpathogen.
Susu dapat dipasteurisasi dengan 2 cara. Metode yang satunya
adalah susu dipanaskan pada suhu 63oC selama 30 menit. Kuantitas
besar susu sekarang ini harus dilakukan flash pasteurization atau
high-temperature-short-term (HTST) pasteurisasi, yang terdiri dari pemanasan
singkat pada suhu 72oC selama 15 detik, kemudian dilakukan
pendinginan. Industry susu terkadang menggunakan ultrahigh-temperature (UHT)
sterilization. Susu dan produknya dipanaskan pada suhu 150oC
selama 1-3 detik. Susu dengan proses UHT tidak membutuhkan kulkas dan dapat
disimpan pada suhu ruangan selama 2 bulan tanpa adanya perubahan rasa. Porsi
kecil Kopi krim yang disediakan di resotran sering disiapkan menggunakan proses
UHT-sterilization.
Banyak objek lebih baik disterilsasi
tanpa menggunakan air dengan dry heat
sterilization. Benda yang disterilisasi ditempatkan di oven pada suhu
160-170oC selama 2-3 jam. Kematian mikroba merupakan hasil dari
oksidasi sel yang konstituen dan perubahan sifat protein. Meskipun pemanasan
dengan udara kering tidak seefektif moist
heat. Spora Clostridium botulinum
dibunuh dalam 5 menit pada 121oC dengan moist heat tetapi hanya setelah 2 jam pemanasan dry heat 160oC memiliki
beberapa keuntungan. Dry heat tidak melelehkan peralatan kaca dan instrument logam
seperti pada moist heat. Banyak lab
mensterilkan kaca petri dan pipet dengan dry
heat. Meskipun dengan keuntungan ini, sterilisasi dengan dry heat prosesnya lambat dan tidak
cocok dengan material yang sensitif terhadap panas seperti plastik dan
benda-benda karet.
Temperatur Rendah
Meski penekanan kita berfokus pada penghancuran
mikroorganisme, namun metode mengekang pertumbuhannya dapat dikontrol dengan
mudah dengan menggunakan freezer atau kulkas. Pendekatan ini penting untuk
makanan mikrobiologi (hal 970). benda yang dibekukan pada suhu -20oC
atau lebih rendah akan menghentikan pertumbuhan mikroba Karena suhu rendah dan
ketiadaan cairan air. Beberapa mikroorganisme akan mati Karena pengkristalan es
mengganggu membrane sel. Tetapi pembekuan tidak menghancurkan mikroba. Faktanya
pembekuan sangat bagus untuk menyimpan sampel mikroba apabila dilakukan dengan
benar, dan banyak lab memiliki freezer untuk menyimban tabung pada suhu -30
hingga -70oC. Karena makanan beku mengandung mikroorganisme, maka
harus segera dikonsumsi setelah dibekukan guna menghindari basi pertumbuhan
pathogen.
Pembekuan mengurangi pertumbuhan dan reproduksi
mikroba, tetapi tidak dapat menahan sepenuhnya. Untungnya pathogen bersifat
mesophilic dan tidak tumbuh pada suhu dibawah 4oC. benda yang
dibekukan dapat hancur karena pertumbuhan mikroorganisme psychronophilic dan
psychrotrophic, khususnya apabila terdapat air. Oleh Karena itu pembekuan
adalah teknik yang bagus hanya pada penyimpanan makanan dalam waktu yang tidak
terlalu lama.
Filtrasi
Filtrasi adalah cara yang sangat baik untuk mengurangi
populasi mikroba dalam larutan yang mengandung material sensitive panas, dan
terkanang digunakan untuk mensterilisasi larutan. Dibanding dengan secara
langsung menghancurkan mikroorganisme yang sudah terkontaminasi, filtarsi hanya
menghilangkan mereka. Ada dua jenis filtrasi. Depht Filter terdiri dari material yang berserat dan
butiran-butiran yang saling mengikat menjadi lapisan tebal yang terisi dengan
saluran yang berputar pada diameter kecil. Larutan yang mengandung mikroorganisme
diserap melalui lapisan ini dengan vakum, dan sel mikroba dihilangkan dengan
penyaringan fisikal atau entrapment(penangkapan) dan juga pengisapan ke luar
material filter. Depth filter terbuat dari diatomaceous earth (Berkefield
filters), porcelain tanpa glasir (Chamberlain filters), asbestos dan material
sejenis lainnya.
Membrane filters
dapat menggantikan depth filter untuk berbagai kegunaan. Filter bundar ini
berupa membrane berpori, setebal 0,1 mm, terbuat dari cellulose acetate,
cellulose nitrate, polycarbonate, polyvinylidene fluoride, atau bahan sintetis
lain. Meski terdapat banyak macam ukuran lubang pori membaran dengan pori
sekitar 0,2 u.m
diameternya digunakan untuk menghilangkan sel vegetative, namun bukan virus,
dari larutan dengan volum 1 mili hingga liter. membran kemudian diletakkan di
pegangan khusus (gambar 7.4) dan sering didahului dengan depth filter yang
terbuat dari kaca fiber guna menghilangkan partikel besar yang dapat menyumbat
membrane filter. Larutan kemudian ditarik atau dipaksa melewati filter dengan
vakum atau tekanan yang kuat dari suntikan, pompa perislaltic, atau botol gas
nitrogen, dan dikumpulkan dalam wadah yang disterilisasi sebelumnya. Membrane
filter menghilangkan mikroorganisme dengan cara menyaring mereka dengan ayakan
guna memisahkan partikel pasir yang besar dari yang kecil (gambar 7.5). filter
ini digunakan untuk mensterilisasi secara parmatik, larutan ophthalmic, tabung
uji, minyak, antibiotic, dan larutan sensitive panas lainnya.
Udara juga bias disterilisasi dengan filtrasi. Dua
contoh yang umum adalah masker operasi dan steker kapas pada wadah dengan cara
memasukkan udara namun mengeluarkan mikroorganisme. Laminar flow biological safety cabinets menggunakan high-efficiecy particulate air (HEPA)
filters, yang dapat menghilangkan 99,97% dari 0,3 u.m partkel, adalah
system filtrasi udara yang paling penting. Laminarflow biological safety
cabinets memasksa air lewat melalui filter HEPA, kemudain memprojeksikan tirai
secara vertical hingga udara dapat lewat melalui celah cabinet. Hal ini
melindungi pekerja dari mikroorganisme yang ditangani dengan cabinet dan
mencegah ruangan dari kontaminasi. (gambar 7.6). seseorang akan menggunakan
cabinet ini ketika bekerja dengan agent/perantara seperti Mycobacterium tuberculosis, virus tumor, dan penggabungan DNA. Hal
ini juga diterapkan di lab ataupun pabrik. Seperti pabrik obat-obatan.
Gambar 7.4
Membrane Filter Sterilization, sebuah membrane
filter untuk mensterilkan volume larutan. (a) Cross section dari unit membran
filter. Beberapa membrane digunakan untuk meningkatkan kapasitas. (b) set
komplit dari filtering. Larutan yang akan diterilisasi diletkkan di tabung
Erlenmeyer, 1, dan dipaksa melewati
filter dengan pompa peristaltic, 2,
larutan disterilisasi dengan mengalirkan mealaui unit membran filter, 3, dan menuju ke container yang steril.
Berbagai jenis filtering juga tersedia.
Gambar 7.5 Membrane
Filter Types, (a) Bacillus megaterium pada membrane nilon Ultipor dengan tingkat
pelenyapan bakteri 0,2u.m (x 2000). (b) Enterococcus
faecalis yang ada pada membran filter polycarbonate dengan pori 0,4u.m
(x5900).
Radiasi
Terdapat berbagai jenis radiasi dan terdapat banyak
cara pula radiasi merusak dan menghancurkan mikroorganisme yang telah
didiskusikan diatas. Penggunaan fisikal dari ultraviolet dan ionisasi radiasi
pada proses sterilisasi objek akan
dijelaskan setelah ini (pp.130-31).
Ultraviolet
(UV) radiation sebesar 260nm (gambar 6.17) akan sangat berbahaya namun
tidak dapat menembus kaca, film, air dan zat lain secara efektif. Karena
kekurangannya ini, radiasi UV digunakan sebagai agen sterilisasi pada situasi
tertentu saja. Lampu UV terkadang diletakkan di atap ruangan atau pada cabinet
keselamatan biologi guna mensterilisasi udara dan segara yang terpapar diudara.
Karena radiasi UV membakar kulit dan melukai mata, orang yang berkerja di area
tersebut harus mematikan lampu UV ketika area sedang digunakan. Unit komersial
UV tersedia untuk pemrosesan air. Pathogen dan mikroorganisme lain akan hancur
ketika lapisan tipis/kecil dari air melewati lampu tersebut.
Ionizing
radiation adalah agen sterilisasi yang baik untuk menembus jauh ke dalam
suatu objek. Ia akan menghancurkan bakteri endospore dan sel vegetative,
prokaryotic dan eukaryotic; namun radiasi ionisasi tidak selamanya efektif
terhadap virus. Radiasi Gamma yang berasal dari cobalt 60 digunakan pada
sterilisasi pendingin pada antibiotic, hormone, benang bedah, dan barang
plastik habis pakai seperti suntikan. Radiasi gamma juga digunakan untuk
mensterilisasi dan “pasteurisasi” daging dan makanan lain. Radiasi ini dapat
melenyapkan ancaman dari pathogen seperti Escherichia
coli 0157:H7, Staphylococcus aureus,
dan Campulobacter jejuni. Badan
administrasi obat dan makanan serta WHO telah menyetujui penyinaran makanan
dengan radiasi dan dianggap aman. Pusat radiasi komersial beroperasi pada
Tampa, Florida. Namun, proses ini belum diterapkan secara luas di U.S Karena
biaya dan kekhawatiran terhadap efek dari radiasi gamma terhadap makanan.
Pemerintah U.S saat ini menyetujui penggunaan radiasi dalam proses pengolahan
daging unggas, daging sapi, daging babi, daging sapi muda, daging kambing,
buah-buahan, sayuran dan berbagai rempah. Kemungkinan proses ini akan lebih
jauh dipakai dimasa yang akan datang.
7.5 Pengguna Agent/Perantara
Kimia dalam Proses Pengendalian.
Meski terkadang objek di disinfeksi dengan agen
fisikal, agen kimia juga sering dipakai untuk proses disinfeksi dan antisepsis.
Banyak factor yang mempengaruhi kefektifan dari senyawa kimia disinfektan dan
antiseptic seperti dijelaskan sebelumnya. Factor seperti mikroorganisme apa
yang mungkin akan ditemukan, konsentrasi serta sifat alami dari disinfectant yang
digunakan, serta lamanya proses penanganan harus diperhitungkan. Permukaan yang
kotor harus dibersihkan sebelum disinfectant atau antiseptic dipakai.
Penggunaan secara wajar dari agen kimia juga penting dalam keselamatan di rumah
sakit dan lab. (kotak 7.2). harus dicatat bahwa senyawa kimia juga dipakai
untuk mengekang pertumbuhan mikroba pada makanan, hal ini dielaskan pada
chapter makanan mikrobiologi (971-72).
Banyak senyawa kimia berbeda digunakan sebagai
disinfectant, masing-masing memilki kelebihan dan kekurangan tersendiri. Dalam
memilih agen, sangat penting untuk mengingat karakteristik dari disinfectant
yang ingin dipakai. Secara ideal, disinfectant harusnya efektif melawan
berbagai jenis agen penyebab infeksi (bakteri gram-positif, gram-negatif,
bacteria asam, bateri endospore, jamur dan virus) pada zat yang encer dan
hadirnya benda organic. Meskipun senyawa ini bersifat racun terhadap agen
pembawa penyakit, senyawa ini tidaklah berbahaya bagi manusia ataupun tidak
korosif pada material umum. Keseimbangan antara rendahnya tingkat toksistas dan
efektifitas terhadap hewan sangat susah dicapai. Beberapa senywa digunakan
meskipun memiliki efektifitas yang rendah dikarenakan mereka bersifat nontoxic.
Disinfectan harus dalam keaadan stabil ketika disimpan, tidak berbau atau
memiliki bau yang harum, larut dalam air dan lipid untuk menembus
mikroorgaisme, dan memiliki tegangan yang rendah sehingga dapat masuk dari
celah permukaan, dan jika memungkinkan disinfectant ini tidaklah berharga
mahal.
Masalah yang sering muncul adalah
penggunaan secara berlebih dari triclosan dan germicida lainnya. Agen
antibakteri sekarang ini dapat ditemukan di produk seperti, deodorant, pencuci
mulut, sabun, nampan, dan mainan bayi. Triclosan terdapat dimana-mana,
sayangnya kita sekarang ini telah melihat munculnya bakteri yang resistan
terhadap triclosan. Pseudomonas
aeruginosa secara aktic memompa antiseptic keluar dari sel. Bakteri
sepertinya merespon penggunaan antiseptic berlebih seperti halnya mereka
bereaksi terhadap penggunaan antibiotic berlebih (pp. 818-20). Sekarang ini
terdapat beberapa bukti yang menyatakan bahwa penggunan triklosan secara
berlebih dapat meningkatkan frekuensi dari ketahanan bakteri terhadap
antibiotic. Oleh Karena itu penggunaan antiseptic secara berlebih tidaklah
baik.
Sifat dan kegunaan dari beberapa
kelompok disnfetan dan antiseptic yang umum akan disurvei nanti. Banyak
karakteristik telah diringkas pada tabel 7.4 dan 7.5. struktur dari beberapa
agen yang umum ditemui terdapat di gambar 7.7
Tabel 7.4 Tingkat
aktifitas dari germicides tertentu
Tabel 7.5 Relativitas
kemanjuran dari disinfectant dan antiseptic yang umum dipakai
Gambar 7.7 Disinfectant dan Antiseptics.
Struktur dari beberapa disinfectant dan antiseptic yang umum dipakai.
Phenolics
Fenol secara umum digunakan pada antiseptic dan
disinfectant, pada tahun 1867 Joseph Lister memakai fenol guna mengurangi
resiko infeksi ketika operasi. Dewasa ini fenol dan fenolik (turunlik
bersifatan fenol) seperti cresols, xylenols dan orthophenylphenol digunakan
sebagai disinfectant pada lab dan rumah sakit. Disinfektan yang umum ialah
Lysol yang terbat dari campuran fenolik.
Fenolik bekerja dengan cara mengubah sifat protein dan merusak sel
membrane. Mereka memiliki beberapa manfaat sebgai disinfectant. Fenolik
bersifat tuberculocidal, efektif pada permukaan setelah pemakaian yang lama.
Namun ia juga berbau kurang sedap dan dapat menyebabkan iritasi kulit.
Alkohol
Alkohol adalah disinfektan dan antiseptic yang paling
umum digunakan. Ia bersifat bactericidal dan fungicidal namun tidak sporicidal;
beberapa virus yang mengandung lipid juga dihancurkan. Dua jenis germicida
alcohol yang sering dipakai ialah ethanol dan isopropanol, umumnya memiliki
konsentrasi 70-80%. Mereka bekerja dengan cara mengubah sifat protein dan
meleburkan membrane lipid. Rendam selama 10-15 menit akan cukup untuk
disinfeksi thermometer dan instrument kecil lainnya.
Halogen
Halogen adalah bagian dari lima elemen (fluorine,
chlorine, bromine, iodine, dan astatine) dalam kelompok VIIA dari tabel
periodik. Mereka berupa molekul diatomik dalam keadaan bebas dan berbentuk
seperti senyawa garam dengan sodium dan logam lainnya. Halgen iodin dan
chlorine merupakan agen mikroba yang penting. Iodine digunakan sebagai
antiseptic kulit dan membunuh dengan cara mengoksidasi sel dan iodinasi sel
protein. Pada konsentrasi yang lebih tinggi. Dapat juga membunuh beberapa
spora. Iodine sering digunakan sebagai perasa iodine, 2% atau lebih jumlah
iodine dalam larutan air-ethanol pada potassium iodide. Meskipun efektif sebgai
antiseptic, kulit juga dapat terluka, terdapat sisa noda, dan menyebabkan
alergi iodine. Sekarang ini iodine lebih bersifat kompleks dengan carrier
organik hingga membentuk iodophor.
Iodophor adalah air yang larut, stabil dan tidak berbetuk, dan melepaskan
iodine secara perlahan guna meminimalisir terbakarnya kulit dan iritas. Mereka
sering digunakan di rumah sakit untuk pengoprasian kulit dan disinfeksi.
Beberapa merk popular seperti Wecodyne untuk disinfeksi kulit dan Betadine untuk
mengobati luka.
Chlorine adalah disinfetant yang berupa kumpulan
tampungan air dan kolam renang dan juga dipakai pada produk susu dan makanan
pabrik. Chlorine dapat berupa gas, sodiu hyphochlorite, atau calcium
hypochlorite, yang menghasilkan asam hypochlorous (HClO) dan atom oksigen.
Hasilnya ialah oksidasi material sel dan hancurnya bakteri vegetative dan
jamur, meski tidak menghancurkan spora.
Kematian seluruh mikroorganisme umumnya terjadi pada
masa 30 menit. Semenjak material organic bercampur dengan chlorine sehingga
bereaksi terhadap chlorine dan produk-produknya. Masalah yang mungkin muncul
ialah chlorine bereaksi pada senyawa organic guna membentuk carcinogenic
trihalomethanes, yang harus diperhatikan apabila terdapat pada air minum. Ozone
terkadang digunakan sebagai alternative klorin dai Eropa dan Canada.
Chlorine juga berupa disinfectant
yang baik untuk penggunaan individual Karena bersifat efektif, tidak mahal, dan
mudah digunakan. Sejumlah kecil dari air minum dapat di disinfeksi dengan tablet
halazone. Halazone (parasulfone dichloramidobenzoic acid) secara perlahan
melepaskan chloride ketika ditambah air dan men disinfeksikannya dalam waktu
sekitar 30 menit. Umum digunakan oleh perkemahan pada keadaan kurangnya air
yang bersih.
Larutan Chlorine merupakan
disinfectant alat-alat lab dan rumah. Kombinasi deterfen disinfektan dapat
disiapkan jika 1/100 pemutih diencerkan (missal 1.3 fl oz dari Clorox atu Purex
dalam 1 gal atau 10ml/liter) dikombinasikan dengan deterjen nonionic yang cukup
(sekitar 1oz/gal atau 7.8ml/liter) guna mendapatkan konsentasi detergen sebesar
0,8%. Campuran ini akan menghilangkan noda, debu dan bakteri.
Heavy Metal (Logam Berat)
Selama bertahun-tahun ion dari logam berat seperti
merkuri, perak, arsenic, zinc, dan tembaga digunakan sebagai germisid. Namun
sekarang ini telah digantikan dengan germisida yang tidak terlalu toxic dan
lebih efektif (banyak logam berat bersifat bacteriostatic dan bactericidal).
Namun terdapat beberapa pengecualian. 1% larutan perak nitrat diteteskan di
mata bayi guna mencegah ophthalmic honorrhea (dalam banyak rumah sakit,
erythromycin digunakan sebagai pengganti perak nitrat Karena sangat efektif
terhadap Chalnydia dan Neisseria). Silver sulfadiazine
digunakan dalam pembakaran. Tembaga sulfat efektid sebagai algicide pada danau
dan kolam renang.
Logam berat dicampur dengan protein,
sering dengan kelompok sulfhydryl, akan mematikan mereka. Ia juga dapat
mengendapkan sel protein.
Quaternary Ammonium
Compounds (Senyawa Kuarter Ammonium)
Detergents
(latin: detergere, menghapus atau
mengusir) adalah molekul organic yang beperan sebagai agen/senyawa pembasah dan
emulsifiers Karena mereka bersifat polar hydrophilic dan nonpolar hydrophobic.
Karena sifat ampiphatik mereka (lihat bagian 3.2), deterjen melarutkan residue
yang tidak dapat larut sebelumnya dan sangat efektif dalam membersihkan agent.
Mereka berbeda dengan sabun yang merupakan turunan dari lemak.
Meskipun detergen anionic memiliki
sifat antimikroba, hanya detergen cationic yang efektif dipakai sebgai
disinfectant. Disinfectant yang popular adalah senyawa kuarter ammonium yang
ditandai dengan kuarter nitrogen yang bersifat posif dan merupakan rantai
panjang hydrophobic aliphatic (gambar 7.7) mereka merusak membrane mikroba dan
dapat merubah sifat protein.
Detergen cationic sepertei
benzalkonium chloride dan cetylpyrindinium chloride membunuh sebagian besar
bakteri tetapi bukan M. tuberculosis
datau endospore. Mereka memeliki kelebihan yaitu bersifat stabil, tidak beracun
dan lunak tetapi tidak dapat diaktifkan dengan air keras dan sabun. Detergen
cationic sering dipakai sebgai disinfektan untuk alat makan dan unstrumen kecil
dan sebagai antiseptic kulit beberapa merek yang ada di pasaran seperti
Zephiran mengandung benzalkonium chloride dan Ceepryn cetylpyridinium chloride.
Aldehid
Aldehid yang sering dipakai ialah, formaldehyde dan
glutaraldehyde, Karena sangat reaktif terhadap molekul yang menggabungkan asam
nucleic dan protein dan menonaktikan mereka, mungkin didapat dengan melakukan
hubungan silang dan alkylating pada molekul (gambar 7.7). mereka bersifat
sporicidal dan dapat dipakai sebagai pensteril zat kimia. Formaldehyde umumnya
dileburkan dalam air atau alcohol sebelum digunakan. 2% larutan buffer dari
glutaraldehyde efektif dipakai sebgai disinfectant. Dan tidak terlalu
menyebabkan iritasi dibanding dengan formaldehyde dan digunakan untuk men
disinfeksi peralatan lab dan rumah sakit. Glutaraldehyde umumnya memakan waktu
10 menit untuk mendisinfeksi objek, namun membutuhkan waktu 12 jam untuk
menghancurkan spora.
Sterilizing Gases (Gas
pensterilisasi)
Banyak benda sensitive panas seperti piring batu,
plastic habis pakai dan suntukan, mesin pompa jantung dan hati, benang jahit
dan catheters sekarang ini disterilisasi menggunakan gas oksida (gambar 7.7).
ethylene oksida (EtO) bersifat microbicidal dan sporicidal dan membunuhya
dengan cara bergabung denga sel protein. senyawa ini efektif digunakan sebagai
agen pensterilisasi Karena dapat dengan cepat membus lapisan material, bahkan
bungkusan plastik.
Sterilisasi dilakukan dengan alat
ethylene oxide sterilizer, yang tampilannya mirip dengan autoclave, ia
mengontrol konsentrasi EtO, suhu, dan kelembapannya. Karena EtO murni bersifat
explosive, ia umumnya ditambah dengan 10 – 20%
konsentrasi campuran baik itu CO2 maupun
dichlorodifluoromethane. Konsentrasi EtO, kelembapan, dan suhu berpengaruh
terhadap tingkat sterilisasi. Objek yang bersih dapat disterilisasi dalam 5-8
jam pada suhu 38oC atau 3 – 4 jam dengan suhu 54oC ketika
tingkat kelembapan dijaga pada 40 – 50 % dan konsentrasi EtO pada 700mg/liter. Penjenuhan
secara luas dari material yang disterilisasi dapat melenyapkan residu EtO
Karena bersifat sangat toxic.
Betapropiolactone (BPL) juga
terkadang dipakai sebgai gas pensteril. Dalam bentuk larutan diganakan untuk
mensterilkan vaksin dan sera. BPL diuraikan dalam bentuk nonaktif setelah
beberapa jam kemudian akan sangat mudah untuk melenyapkan EtO. Ia juga
menghancurkan mikroorganisme lebih baik dibanding ethylene oxide namun tidak
dapat menembus material dengan baik dan bersifat carcinogenic. Oleh Karena
alasan-alasan ini, BPL tidak sering digunakan dibandingkan dengan EtO.
Dewasa ini hydrogen peroxide dalam
fase-penguapan digunakan untuk dekontaminasi cabinet keselamatan biologis.
7.6 Evaluasi Keaktifan Agen
Antimikroba
Pengujian agen antimikroba adalah
proses yang kompleks dan diregulasi oleh dua badan resmi berbeda. U.S
environmental protection agency mengatur disinfectant, sedangkan agent yang
digunakan kepada manusia dan hewan diatur oleh Food and Drug Administration.
Pengujian agen mikroba sering dimulai dengan proses penyaringan awal untuk
menguji kefektifannya dan pada konsentrasi apa. Baru kemudian dapat dilakukan
tes secara lebih realistik.
Tabel 7.6 Koefisien
Fenol untuk beberapa Disinfectant
Proses penyaringan disinfektan yang
paling umum ialah phenol coefficient
test dimana potensi dari disinfektan dibandingkan dengan phenol. Sejumlah
phonel yang diencerkan dan disinfektan eksperimental disuntikkan pada bakteri Salmonella typhi dan Staphylococcus aureus, kemudaian
diletakkan di air dengan suhu 20 atau 37oC. wadah disinfektan yang
disunttukan ini kemudian dipisahan menjadi bagian regular fresh medium dengan interval 5 menit. Dan diinkubasi selama
2 hari atau lebih. Tingkat keenceran yang dapat membunuh bakteri adalah setelah
terpapar selama 10 menit. Namun dalam menghitung koefisien phenol, tidak boleh
terpapar lebih dari 5 menit. Balasan yang layak untuk setiap ji disinfektan
dibagi dengan phenol untuk mendapat koefisiennya. Misalkan phenol yang
diencerkan sebesar 1/90 dan efektifitas maksimum dari disinfektan X yang diencerkan
ialah 1/450. Maka koefisien phenol adalah 5. Semakin tinggi nilai koefisen
phenol, semakin efektif disinfektan yang diuji. Nilai lebih besar dari 1
berarti disinfektan lebih efektif daripada phenol. Berbagai contoh koefisien
phenol ada pada tabel 7.6
Koefisien fenol yang diuji sangat berguna dalam
prosedur penyaringan namun koefisen phenol dapat juga mengecohkan apabila
dilakukan indikasi langsung dari potensi disinfektan dalam penggunaan normal.
Hal ini dikarenakan koefisien phenol ditentukan dengan kondisi yang sangat
terkontrol dengan tegangan bakteri murni, sedangkan disinfektan umumnya
digunakan pada popuasi yang kompleks dengan adanya zat organik dan berbagai variasi
serta faktor lingkungan seperti
pH, suhu dan jumlah garam.
Guna mengestimasi efektifitas
disinfectant secara realisitis. Dilakukan tes lain, tingkat pemilihan bakteri
yang dihancurkan oleh berbagai agen kimia akan ditentukan dan dibandingkan
secara eksperimental. Use dilution test
dapat juga dilakukan. Silinder stainless steel yang terkondaminasi dengan
spesies bakteri tertentu pada kondisi yang dikontrol. Silinder kemudian
dikeringkan, direndam di dalam disinfectant selama 10 menit, dipindahkan ke tabung
uji, dan diinkubasi selama 2 hari. Konsentrasi disinfektan yang dapat membunuh
organisme dalam sampe dengan tingkat kebenaran 95% dibawah kondisi yang telah
ditentukan. Disinfektan juga diuji dalam
kondisi yang didesain untuk mensimulasi penggunaan secara normal. Teknik ini membolehkan
kita untuk secara akurat menentukan konsentrasi disinfectant yang cocok untuk
situasi tertentu.














Komentar
Posting Komentar